ДИАБЕТИЧЕСКАЯ СТОПА
Синдром диабетической стопы (СДС) объединяет патологические изменения периферической нервной системы, артериального и микроциркуляторного русла костно-суставного аппарата стопы. Это состояние представляет непосредственную угрозу развития язвенно-некротических поражений и гангрены стопы.
В группу риска развития диабетической стопы входят следующие группы пациентов:
- с нарушением периферической чувствительности любого генеза;
- с окклюзирующими заболеваниями периферических артерий;
- с деформациями стоп любого генеза;
- слепые и слабовидящие;
- одинокие пациенты, люди пожилого возраста;
- злоупотребляющие алкоголем.
Клинические формы синдрома диабетической стопы
В настоящее время предложен ряд классификаций синдрома диабетической стопы, в основу которых положены представления об основных причинах развития этого осложнения диабета, учитывается тяжесть поражения, оценка размеров раневого дефекта и выраженности инфекционного процесса.
В основу классификации, предложенной Diabetic Foot Study Group и утверждённой Консенсусом по диабетической стопе 2015 года, положены представления о патогенезе раневого дефекта стопы при сахарном диабете.
Согласно ей выделяют следующие клинические формы синдрома диабетической стопы:
- нейропатическая форма СДС;
- ишемическая форма СДС;
- нейроишемическая форма.
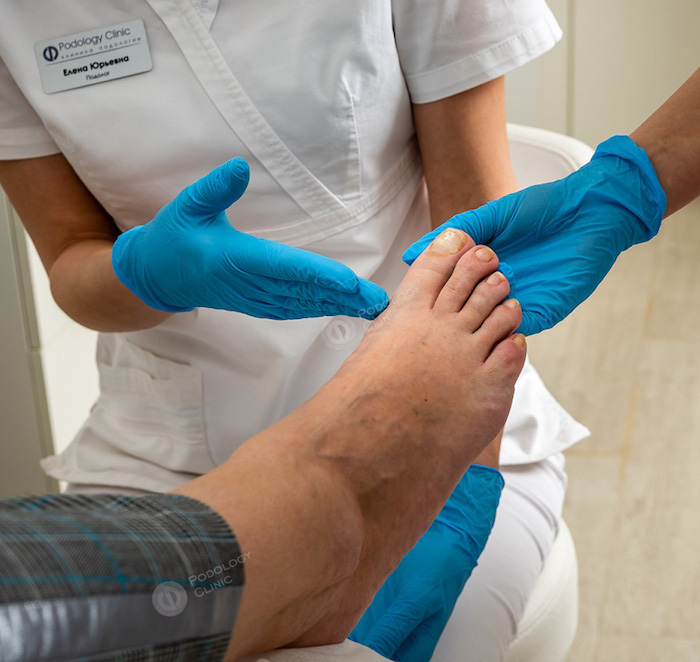
По глубине язвенного дефекта поражения можно разделить на 5 степеней (классификация Wagner):
- 0 степень — интактная неповреждённая кожа;
- I степень — поверхностная язва (процесс захватывает эпидермис, дерму);
- II степень — инфекционный процесс захватывает кожу, подкожную клетчатку, мышцы;
- III степень — глубокая язва, абсцесс, остеомиелит, септический артрит;
- IV степень — сухая/влажная гангрена: некроз всех слоёв кожи отдельных участков стопы (например, часть пальца/палец);
- V степень — сухая/влажная гангрена части стопы/всей стопы.
Симптомы диабетической стопы
Повреждение нервов (диабетическая нейропатия) может вызывать онемение, покалывание, боль и потерю чувствительности в нижних конечностях. Из-за потери чувствительности пациент может не заметить порезы, волдыри, язвы на ногах. Присоединение инфекции ухудшает его состояние: раны плохо заживают, поскольку кровоток в ногах затруднён из-за повреждения кровеносных сосудов. Инфекция и плохой кровоток приводят к некротизации кожи, мышц и других тканей (гангрене) и необходимости ампутации пострадавшей конечности — для предотвращения распространения тяжёлой инфекции.
К симптомам диабетической стопы относятся:
- любые изменения цвета кожи или ногтевых пластин стоп: порезы, волдыри, мозоли, язвы, истончение кожи или шелушение, утолщение или расслаивание ногтей, изменение их формы и цвета, кровоизлияния под ногтевыми пластинами;
- потеря чувствительности кожи на поражённом участке (тактильного, температурного и болевого восприятия);
- покалывание, жжение, боль в стопах, отёки;
- выпадение волос на поражённом участке;
- изменения локальной температуры стоп и голеней;
- длительно не заживающие трофические язвы на стопах (от нескольких недель до нескольких лет).
Диагностика синдрома диабетической стопы
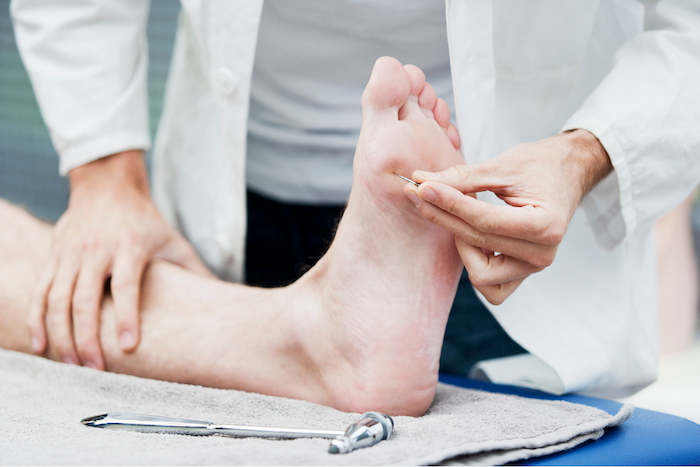
Наличие и выраженность болевого синдрома зависят от состояния периферической чувствительности (возможно снижение вплоть до полной анестезии вследствие диабетической сенсорной нейропатии), уровня локальной ишемии и тяжести присоединившейся инфекции.
При сборе анамнеза подолог обращает внимание на длительность течения сахарного диабета (СД), наличие других поздних осложнений этого заболевания. СД второго типа — скрытое малосимптомное заболевание, которое часто диагностируется при обследовании пациента с уже развившимся тяжёлым гнойно-некротическим поражением стопы. Кроме того, на скорость заживления раневых дефектов могут влиять сопутствующие, непосредственно не связанные с СД заболевания: сердечная и дыхательная недостаточность, онкологические заболевания, алиментарная недостаточность, терапия глюкокортикоидами и иммуносупрессантами.
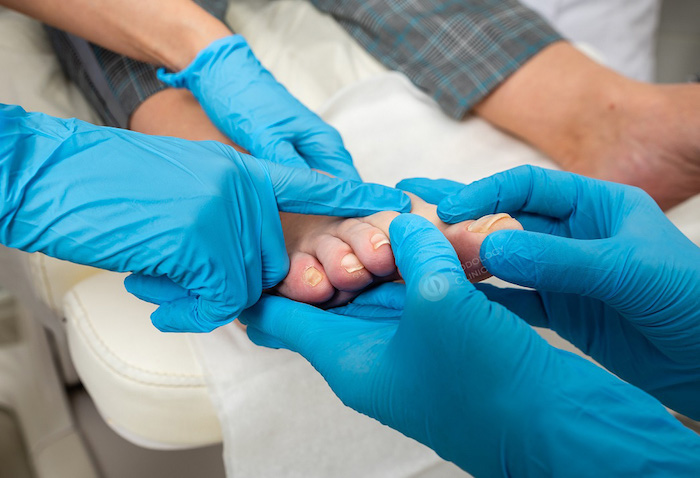
Во время физикального осмотра — осмотра стоп, голеней и пальпации — подолог обращает внимание на состояние и цвет кожных покровов (сухие, влажные, бледные, розовые, гиперемированные), пальпаторно определяет их температуру (холодные, тёплые, горячие), оценивает состояние ногтевых пластин, поскольку онихомикоз (грибковое поражение) может являться дополнительным источником инфекции. Асимметрия цвета и температуры кожи обеих стоп может служить первым признаком имеющегося нарушения. Результаты такого осмотра могут помочь составить первое мнение о возможной клинической форме синдрома диабетической стопы.
Далее подолог проводит оценку состояния периферического артериального кровотока. Значимая артериальная недостаточность может быть исключена при наличии хорошо пальпируемого пульса на тыльной артерии стопы, передней и задней большеберцовых артериях или лодыжечно-плечевом индексе (ЛПИ) >0,9. ЛПИ >1,3 свидетельствует о ригидности артериальной стенки. У пожилых пациентов или у лиц с ЛПИ >1,2 состояние артериального кровотока должно быть подтверждено уровнем артериального давления в пальцевой артерии (величиной пальце-плечевого индекса, ППИ) или данными транскутанной оксиметрии (ТсрО2 >40 мм рт. ст.). Ультразвуковое дуплексное сканирование артерий подтверждает артериальную окклюзию, выявляет её анатомическую локализацию и протяжённость.
Наличие диабетической нейропатии устанавливается на основании определения тактильной чувствительности с помощью 10 г монофиламента. Достоверность полученных результатов повышается при дополнительной оценке других видов чувствительности (вибрационной с помощью градуированного камертона 128 Гц или биотезиометра) и/или сухожильных рефлексов.
«Золотым стандартом» оценки состояния костей и суставов является рентгенография, позволяющая с высокой достоверностью определять очаги остеолиза (остеомиелита). Мультиспиральная компьютерная томография помогает уточнить локализацию и размеры остеомиелитического очага при планировании объёма оперативного вмешательства. Однако эти методы визуализации неинформативны в диагностике острой стадии диабетической остеоартропатии. В этом случае целесообразно использование магнитно-резонансной томографии, метод позволяет выявить отёк костного мозга в зоне предполагаемого поражения. Наиболее простым, доступным и достаточно информативным методом диагностики острой стадии ДОАП является инфракрасная термометрия. Разница температуры над поражённым и контлатеральным непоражённым суставом в 2 и более градусов Цельсия позволяет с высокой долей вероятности диагностировать это осложнение и своевременно начать адекватное восстановление.
Основным методом диагностики инфекционного процесса в ране является бактериологическое исследование. Для анализа берут образцы тканей из разных участков, так как микрофлора может различаться в разных областях дефекта. У пациентов с нейроишемической и ишемической формой СДС выявляют не только аэробные, но и анаэробные микроорганизмы и определяют их чувствительность к современным антибактериальным препаратам. Клинически значимым считается содержание бактериальных тел выше 1 х 106 на грамм ткани или обнаружение β-гемолитического стафилококка.
Оценка состояния углеводного и липидного обмена также является абсолютно необходимым компонентом обследования. Проводится исследование таких параметров, как уровень гликированного гемоглобина А1с (HbA1c), уровень пре- и постпрандиальной гликемии, общего холестерина, холестерина ЛПНП сыворотки крови. Коррекция нарушений углеводного обмена у пациента с СДС должна проводиться параллельно с восстановлением раневого дефекта. Для пациентов с нейроишемической формой СДС обязательным является назначение гиполипидемической терапии статинами и нормализация артериального давления.
Профилактика диабетической стопы
Основное условие успешного лечения трофических язв у пациентов как с нейропатической, так и с ишемической и нейроишемической формами синдрома диабетической стопы — обеспечение полной разгрузки поражённой области. Возможными методами разгрузки являются разгрузочный полубашмак, индивидуальная разгрузочная повязка (Total Contact Cast — наиболее эффективный метод разгрузки поражённой зоны стопы) и костыли. Адекватное использование кресла-каталки не всегда возможно, особенно в амбулаторных условиях.
Пациентам группы высокого риска развития трофических язв стоп (значимая артериальная недостаточность, тяжёлая нейропатия, язвы стоп в анамнезе, грубый гиперкератоз) показано постоянное ношение профилактической обуви для больных диабетом, а пациентам, перенёсшим ампутацию в пределах стопы, — сложной ортопедической обуви.
Параллельно с разгрузкой поражённой зоны должна проводиться первичная обработка раны, направленная на удаление всех некротизированных и нежизнеспособных тканей и подготовку раневого ложа к заживлению. Возможно использование хирургического, ферментного, механического, ультразвукового методов или их комбинации. Метод обработки выбирается индивидуально, исходя из состояния раны, общего состояния пациента. После проведения обработки рану закрывают стерильной атравматичной повязкой. В процессе лечения может возникнуть необходимость в повторном проведении обработки раневого дефекта.
Важнейшим аспектом лечения трофических язв у пациентов с СДС служит контроль раневой инфекции. Первым этапом является полное удаление некротизированных и нежизнеспособных тканей хирургическим методом.
Могут быть использованы как классический метод хирургической обработки, так и современные технологии:
- гидрохирургическое оборудование;
- ультразвуковая кавитация;
- лазерная вапоризация;
- фотодинамическая терапия.
При наличии критической ишемии конечности проведение хирургической обработки раны опасно, так как может привести к расширению зоны некроза. В случае проведения адекватной обработки раневого дефекта эпителизация должна начаться в течение двух недель при условии соблюдения оптимального режима разгрузки поражённой области.
Если этого не произошло, показано проведение бактериологического исследования тканей раны. Дальнейшие терапевтические мероприятия будут зависеть от результатов этого исследования.
При выявлении β-гемолитического стафилококка и/или содержания микробных тел более 1 х 106 на грамм ткани показана повторная хирургическая обработка раневого дефекта и местное использование антисептика. При достижении бактериального баланса применение антисептика прекращают во избежание цитотоксического эффекта и бактериальной резистентности. При активном инфекционном процессе (фебрильная лихорадка, лейкоцитоз, гнойный раневой экссудат, гиперемия и гипертермия мягких тканей поражённой области) показано проведение системной антибактериальной терапии с учётом характера и чувствительности микрофлоры. Важным условием при выборе антибактериального препарата является предварительная оценка азотовыделительной функции почек (по скорости клубочковой фильтрации, СКФ). При СКФ < 45 мл/мин./1,73 м2 доза антибактериального препарата должна быть редуцирована.
При подозрении на наличие остеомиелита проводится дополнительное обследование (зондирование раны, рентгенография, МСКТ). При подтверждении диагноза показано хирургическое вмешательство — удаление поражённой кости с последующей антибактериальной терапией в течение 2–4 недель. После достижения бактериального баланса раны и заполнения её объёма здоровой грануляционной тканью на 75% и более возможно выполнение пластического закрытия раны местными тканями или аутодермопластики. После лечения проводится постоянная оценка скорости заживления раны. Если раневой дефект за 4 недели не сократился на 40%, тактика лечения пересматривается.
Пациенты с ишемией конечности нуждаются в проведении реваскуляризирующих вмешательств. Показаниями к ангиохирургическому вмешательству (баллонная ангиопластика, баллонная ангиопластика со стентированием, гибридные операции) являются гемодинамически значимые (>85%) стенозы и/или окклюзии артерий нижних конечностей, ведущие к ишемии мягких тканей стопы (ТсрО2 < 30 мм рт. ст.). В периоперационном периоде проводится профилактика контрастиндуцированной нефропатии. При наличии гнойно-некротического очага его первичная санация выполняется до ангиохирургического вмешательства. При невозможности выполнения реваскуляризирующего вмешательства показано назначение препаратов простагландинового ряда.
В острой стадии диабетической остеоартропатии выполняется иммобилизация поражённой конечности с помощью индивидуальной разгрузочной повязки в максимально ранние сроки (в день установления диагноза). Больным с хронической стадией ДОАП показано постоянное ношение сложной ортопедической обуви. Также проводится коррекция сахароснижающей терапии. При наличии показаний (превышение индивидуальных целевых показателей углеводного обмена) коррекция терапии должна проводиться параллельно с профилактикой трофической язвы стопы.
При интенсификации лечения необходимо проводить профилактику тяжёлых гипогликемических состояний. Пациенты с нейроишемической и ишемической формой СДС нуждаются в коррекции возможной дислипидемии, а больные после выполненной ангиопластики — в приёме антитромботиков в течение 6 месяцев. При отсутствии заживления на фоне стандартной терапии можно использовать адъювантные методы (факторы роста, отрицательное давление, электростимуляция). Использование отрицательного давления (NPWT) возможно у пациентов с нейропатической и нейроишемической (после восстановления кровотока) формой синдрома. Абсолютно противопоказано использование NPWT у больных с выраженной ишемией конечности (TcpO2 < 30 мм рт. ст.), остеомиелитом, флегмоной и гангреной стопы.

